고대안암병원ㆍ일산차병원과 임상시험 절차 진행 예정
아이도트는 인공지능 자궁경부암 스크리닝 솔루션인 ‘써비레이(Cerviray)’가 식품의약품안전처의 3등급 의료영상검출 소프트웨어로 임상시험계획서가 승인됐다고 9일 밝혔다.
이 임상시험계획의 승인에 따라 고려대안암병원 송재윤 교수팀, 일산차병원 김성민 교수팀과 함게 본격적인 임상시험 절차를 진행한다.
박민찬 연구소장은 “아이도트의 써비레이(Cerviray)는 국내 타 인공지능 영상 검진 솔루션과는 달리 ▲단순한 정상, 비정형, 저등급병변, 고등급병변 구분이나 ▲백색상피, 모자이크, 비정형혈관 인식 등이 아닌 환자마다 각기 다른 병변의 질감·모양·위치를 종합하고, 표준화 기술을 통해 세계보건기구의 기준에 부합하는 더욱 세분화된 판독 모델로 고도화했다”고 밝혔다.
특히“저등급병변의 경우 육안으로 놓칠 확률이 높은 작은 병변이라도 인공지능이 오차범위 3% 이내로 위치를 탐지하고, 이 작은 병변들을 근거로도 실제 임상 교수진이 수십 년의 경험을 바탕으로 종합적 판단을 내리는 진단 프로세스를 그대로 AI에 이식했다”고 언급했으며 “이러한 임상시험 통계 절차는 국내 유일한 인공지능 기반 영상판독 임상시험이 될 것”이라고 덧붙였다.
또한 박민찬 연구소장은 “임상통계 절차를 글로벌 경쟁력 차원에서 정의함으로써 국내뿐 아니라, 해외에서도 그 신뢰도가 한층 강화될 것으로 내다봤다”고 말했다.
이어 “아이도트는 이미 국제표준인증인 ISO13485, ISO9001뿐 아니라 유럽 CE 인증도 모두 확보한 상태로, 국내 식약처 인증이 완료되면 국내 식약처 임상 결과를 요구하는 국가들에게 공신력을 제공할 수 있으며, 한창 논의 중인 일본·북미·유럽국가의 인증 과정에서도 검증이 됨으로 곧바로 글로벌 시장 진입을 완료할 계획이다”라고 밝혔다.
아이도트의 전략적 투자사 및 파트너인 한국필의료재단 정영묵 이사는 “이미 국내의 기존 로컬 산부인과를 대상으로 사용성 및 효용성을 확인했고, 국내 식약처 인증이 완료되는 시점에 도입 의사를 밝힌 병원에게 순차적으로 공급될 것”이라며 “이는 국내에서 유일하게 인공지능 의료기기를 1·2차 병원에 확산을 한다는 측면에서 병원과 환자가 모두 윈윈할 수 있는 훌륭한 계기가 될 것”이라고 말했다.Source: https://8xbets-vn.com/tu-quy-co-chat-duoc-doi-heo-khong/
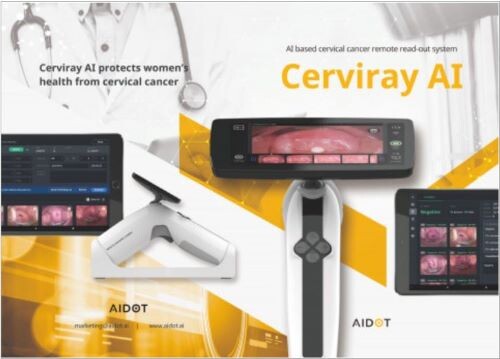 |
| ▲써비레이 AI 시스템 이미지 (사진= 아이도트 제공) |
아이도트는 인공지능 자궁경부암 스크리닝 솔루션인 ‘써비레이(Cerviray)’가 식품의약품안전처의 3등급 의료영상검출 소프트웨어로 임상시험계획서가 승인됐다고 9일 밝혔다.
이 임상시험계획의 승인에 따라 고려대안암병원 송재윤 교수팀, 일산차병원 김성민 교수팀과 함게 본격적인 임상시험 절차를 진행한다.
박민찬 연구소장은 “아이도트의 써비레이(Cerviray)는 국내 타 인공지능 영상 검진 솔루션과는 달리 ▲단순한 정상, 비정형, 저등급병변, 고등급병변 구분이나 ▲백색상피, 모자이크, 비정형혈관 인식 등이 아닌 환자마다 각기 다른 병변의 질감·모양·위치를 종합하고, 표준화 기술을 통해 세계보건기구의 기준에 부합하는 더욱 세분화된 판독 모델로 고도화했다”고 밝혔다.
특히“저등급병변의 경우 육안으로 놓칠 확률이 높은 작은 병변이라도 인공지능이 오차범위 3% 이내로 위치를 탐지하고, 이 작은 병변들을 근거로도 실제 임상 교수진이 수십 년의 경험을 바탕으로 종합적 판단을 내리는 진단 프로세스를 그대로 AI에 이식했다”고 언급했으며 “이러한 임상시험 통계 절차는 국내 유일한 인공지능 기반 영상판독 임상시험이 될 것”이라고 덧붙였다.
또한 박민찬 연구소장은 “임상통계 절차를 글로벌 경쟁력 차원에서 정의함으로써 국내뿐 아니라, 해외에서도 그 신뢰도가 한층 강화될 것으로 내다봤다”고 말했다.
이어 “아이도트는 이미 국제표준인증인 ISO13485, ISO9001뿐 아니라 유럽 CE 인증도 모두 확보한 상태로, 국내 식약처 인증이 완료되면 국내 식약처 임상 결과를 요구하는 국가들에게 공신력을 제공할 수 있으며, 한창 논의 중인 일본·북미·유럽국가의 인증 과정에서도 검증이 됨으로 곧바로 글로벌 시장 진입을 완료할 계획이다”라고 밝혔다.
아이도트의 전략적 투자사 및 파트너인 한국필의료재단 정영묵 이사는 “이미 국내의 기존 로컬 산부인과를 대상으로 사용성 및 효용성을 확인했고, 국내 식약처 인증이 완료되는 시점에 도입 의사를 밝힌 병원에게 순차적으로 공급될 것”이라며 “이는 국내에서 유일하게 인공지능 의료기기를 1·2차 병원에 확산을 한다는 측면에서 병원과 환자가 모두 윈윈할 수 있는 훌륭한 계기가 될 것”이라고 말했다.Source: https://8xbets-vn.com/tu-quy-co-chat-duoc-doi-heo-khong/
메디컬투데이 이대현 (dleogus1019@mdtoday.co.kr)

[저작권자ⓒ 메디컬투데이. 무단전재-재배포 금지]